追尋抗生素耐藥性基因的來源 有望阻截其傳播
對強力抗生素呈耐藥性的「超級細菌」是全球公共衛生的一個計時炸彈。由香港城市大學(香港城大)科學家領導的聯合研究團隊,針對其中一組抗生素耐藥性基因追本溯源,早前發表研究結果,鎖定了其中一種細菌為該組耐藥性基因的潛在來源,并研究其傳播機制,希望有助阻截其傳播。
研究團隊由香港城大賽馬會動物醫學及生命科學院副院長(研究)、傳染病及公共衛生學系教授陳聲教授與內地學者共同領導。研究成果已于科學期刊《自然通訊》(Nature Communications)上發表,題為〈Epidemiological and phylogenetic analysis reveals Flavobacteriaceae as potential ancestral source of tigecycline resistance gene tet(X)〉。
抗生素耐藥性威脅全球
抗生素耐藥性早被世界衛生組織(World Health Organization, WHO)形容為“對目前全球衛生、食品安全和發展的最大威脅之一”。用以治療細菌感染的抗生素因被濫用,令部分細菌出現耐藥性,于是相關感染變得難以治療,導致病人住院時間延長和死亡率上升等后果。
然而,新型冠狀病毒疫情令耐藥性問題進一步擴大。2020年6月,WHO總干事譚德塞便指出,新型冠狀病毒疫情令抗生素的使用增加,進一步加劇細菌對抗生素產生耐藥性的問題。陳教授解釋,其中一個原因是前線醫生在治療新冠病人時,為防止病人同時有其他感染會使用抗生素,因而導致抗生素的使用有所增加。

他表示,醫生在處方抗生素時,理應先由最常用的第一線抗生素開始,若無效,才采用更強的第二線抗生素。然而,目前在世界很多地方,第一線抗生素已經無效,甚至第二線或第三線的抗生素都沒效果,前線醫生已經面臨無藥可用的境地。
陳教授指出,內地的細菌耐藥性問題嚴重,醫護人員或要同時處方幾種抗生素,例如或要用替加環素(tigecycline)和碳青霉烯(carbapenem)雙管齊下,才能有效治療病人。他說:“在內地因為單用碳青霉烯多已對病人無效,替加環素于是成為治療由多重耐藥性細菌引發嚴重感染的最后一道防線。"
然而,替加環素用量上升,同樣衍生細菌耐藥性的問題,世界各地包括內地已有零星對替加環素出現耐藥性的個案。科學家研究后發現了一組替加環素耐藥性基因tet(X),病人如果感染了帶有此基因的病原菌,用替加環素治療的效用會大減,但科學界暫時對tet(X)所知不多。
替加環素耐藥性基因的潛在起源
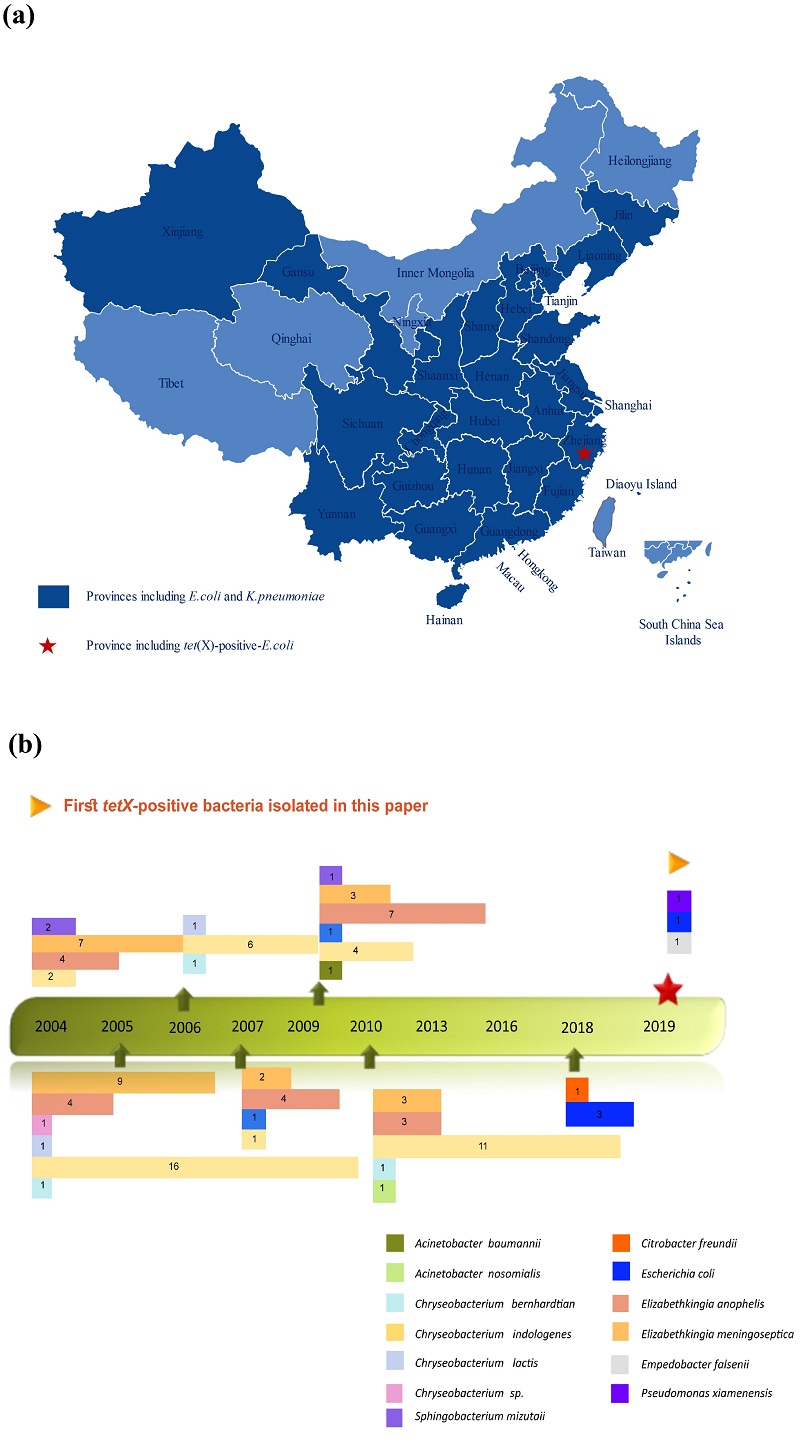
陳教授團隊便就tet(X)展開研究,首次揭示了tet(X)基因的潛在起源和傳播機制。團隊在內地26個省份合共77家醫院,收集了2,997例臨床大腸桿菌和肺炎克雷伯菌的樣本作分析,于當中4個(0.32%)大腸桿菌樣本中發現帶有tet(X)及其變異體,于肺炎克雷伯菌里則沒有發現。
由于該4個大腸桿菌樣本全部采集自浙江省,于是研究人員進一步收集1994至2019年間,于浙江省多家醫院采集到的合共3,692株革蘭氏陰性臨床菌株(clinical Gram-negative bacterial strains)。他們發現當中102株帶有tet(X) 及其變異體,并以黃桿菌科(Flavobacteriaceae)為主要菌種類型,占95株。這95株細菌均對多種抗生素包括替加環素呈耐藥性。
團隊對帶有耐藥性基因的菌株進行全基因組測序及生物信息學分析,發現tet(X)主要位于黃桿菌科的染色體(chromosome)而非質粒(plasmid)上。陳教授解釋說:“tet(X)見于染色體,代表這個基因很可能本來已經存在于黃桿菌內。其實這些耐藥性基因很多都存在于天然生態環境中,只是碰巧人類用了替加環素,tet(X)就剛好發揮作用,令帶有該基因的細菌存活下來。"
另外,研究結果亦發現tet(X)基因的GC含量與黃桿菌科細菌相似,均為大約37%,代表兩者的基因特性很類似。GC含量是指全基因組中兩種物質鳥嘌呤(Guanine, G)和胞嘧啶(Cytosine, C)所占的比例,而一種生物的基因組或者特定DNA、RNA片段,會有特定的GC含量。根據以上的發現,團隊認為黃桿菌科細菌可能是替加環素耐藥性基因tet(X)的潛在祖源(potential ancestral source)。
研究也顯示,來自黃桿菌的tet(X)前體基因(于染色體上最原始的基因)會進化成不同的tet(X)及其變異體。陳教授進一步說:“基因組分析發現,tet(X)的基因片段同時存在于腸桿菌、不動桿菌和黃桿菌中,間接證明了tet(X)可作跨物種傳播。"
有助防控該基因繼續傳播
陳教授總結說:“我們從這個研究了解到tet(X)基因潛在的來源和該基因會怎樣進化,這些重要的信息有助在臨床上防控該基因繼續傳播。我們往后亦應該要多加留意 '源頭'黃桿菌,并密切注意tet(X)基因有否變得更普遍,若有的話,代表基因傳播的情況可能有變。"他表示團隊會作后續的研究,而且成員正按tet(X)基因組各變異體的功能和特點作系統性的分類,便利往后的相關研究。

陳教授和來自浙江大學醫學院附屬第二醫院的陳功祥教授是論文的通訊作者,論文第一作者是香港城大賽馬會動物醫學及生命科學院研究助理董寧博士、來自浙江大學醫學院附屬第二醫院的張嶸教授以及來自中國農業大學的沈張奇教授。而來自香港城大的研究團隊成員還包括研究助理程啟鵬。研究團隊其他成員則來自香港理工大學。
這項研究獲得國家自然科學基金會的資助進行。
DOI number: 10.1038/s41467-020-18475-9
相關故事:
本文已于 “香港城大研創” 微信公眾號發布。
Wechat ID: CityU_Research
