香港城大生物學(xué)家找出令“三陰性乳腺癌”致癌基因活躍的超級增強(qiáng)子
“三陰性乳腺癌”(Triple-negative breast cancer, TNBC)是一種棘手和死亡率高的乳腺癌,目前主要治療手段是化療,但效果欠理想。一支由香港城市大學(xué)(香港城大)生物學(xué)家領(lǐng)導(dǎo)的研究團(tuán)隊(duì),最近便成功找出一組特異的、即針對三陰性乳腺癌的“超級增強(qiáng)子(super-enhancer)”。這些超級增強(qiáng)子會刺激與三陰性乳腺癌有重要關(guān)連的致癌基因,使之變得活躍;若除去這些超級增強(qiáng)子,則能減慢癌細(xì)胞的增長。該項(xiàng)研究成果將有助科學(xué)家針對三陰性乳腺癌研發(fā)出更有效的藥物,提高患者的生存率。
多年以來,乳腺癌的研究大多著眼于找出不同種類乳腺癌的基因突變,但對于“表觀遺傳回路”(epigenetic circuit)如何影響乳腺癌的課題,卻鮮有深入的研究剖析。
表觀遺傳改變:另一種致癌原因
基因突變是指生物遺傳基因DNA一部分或多個(gè)部分的序列突然發(fā)生變化,而“表觀遺傳改變”(epigenetic change)同樣會改變了基因組的DNA,但并非改變了DNA序列,而是從DNA序列上增加或移去了稱為“表觀遺傳標(biāo)記”(epigenetic marks)的特殊標(biāo)記,由此改變了人體內(nèi)蛋白質(zhì)的運(yùn)作。而超級增強(qiáng)子便包含了這種特殊的“表觀遺傳標(biāo)記”,故此假若超級增強(qiáng)子出現(xiàn)異常調(diào)控,便會產(chǎn)生大量可驅(qū)動(dòng)癌細(xì)胞增長的蛋白質(zhì),從而刺激癌癥的形成。
為了找出這些超級增強(qiáng)子怎樣影響三陰性乳腺癌癌細(xì)胞的增長,香港城大生物醫(yī)學(xué)系的兩位科研人員、癌癥生物學(xué)家錢玥明博士與計(jì)算生物學(xué)家王鑫博士聯(lián)手領(lǐng)導(dǎo)一支聯(lián)合研究團(tuán)隊(duì),尋找真相。研究成果已于《自然通訊》(Nature Communications)發(fā)表,題為〈Defining super-enhancer landscape in triple-negative breast cancer by multiomic profiling〉。
王博士帶領(lǐng)的研究團(tuán)隊(duì)使用“多組學(xué)分析”(multiomic profiling)的方法,對超過4,000名乳腺癌病人的臨床資料,以及多達(dá)21個(gè)細(xì)胞系的多層次表觀遺傳基因測序數(shù)據(jù),進(jìn)行深入的數(shù)據(jù)分析,成功針對所有不同種類的乳腺癌,找出其對應(yīng)特異的超級增強(qiáng)子,建立并描繪出一個(gè)調(diào)控網(wǎng)絡(luò)。
癌細(xì)胞增長的重要調(diào)控因子
王博士說:“我們透過綜合分析發(fā)現(xiàn),單是超級增強(qiáng)子的簇群(clustering)已足以助我們辨別出不同種類的乳腺癌??????更重要的是,根據(jù)基因調(diào)控網(wǎng)絡(luò),我們發(fā)現(xiàn)FOXC1這個(gè)基因,是調(diào)控癌細(xì)胞增長及轉(zhuǎn)移的關(guān)鍵轉(zhuǎn)錄因子,而FOXC1正是受到三陰性乳腺癌特異的超級增強(qiáng)子的驅(qū)動(dòng)。此外,F(xiàn)OXC1有助預(yù)測乳腺癌病人的生存率,以及協(xié)助科學(xué)家針對表觀遺傳回路(epigenetic circuits)去研究治療的新策略。”
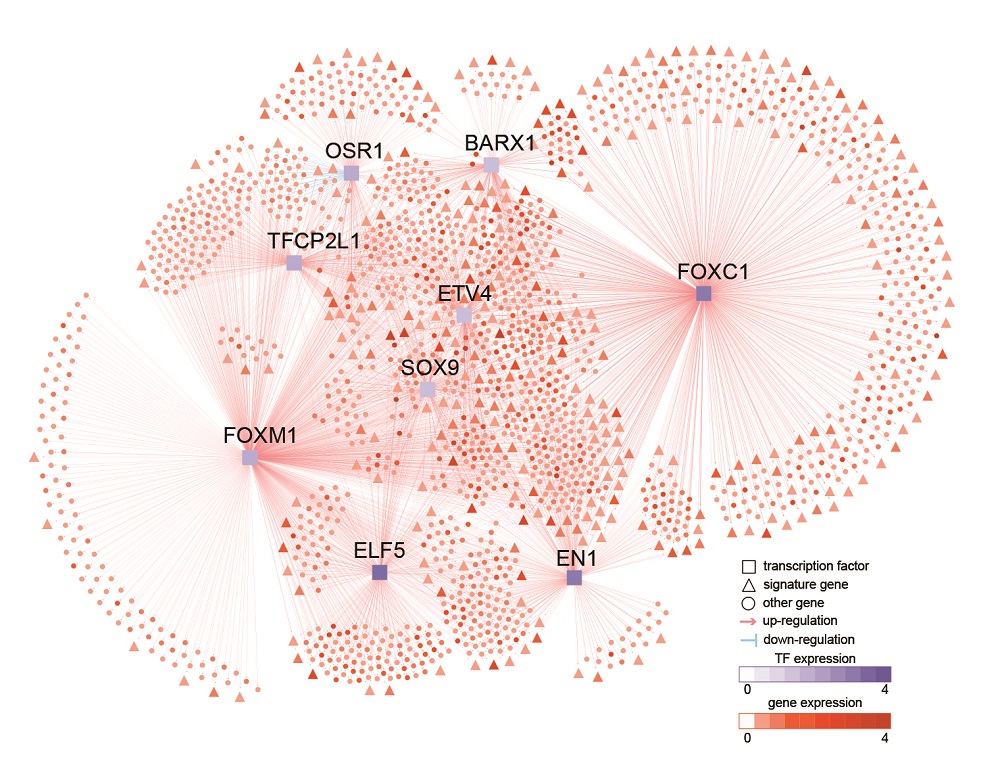
目前科研界已知悉一系列的關(guān)鍵致癌基因如FOXC1及MET,會刺激癌細(xì)胞增長,導(dǎo)致三陰性乳腺癌病人的生存率偏低。然而,究竟為何這些基因在三陰性乳腺癌病人身上會特別活躍,人們則所知甚少。香港城大今次的研究填補(bǔ)了這方面的不足,錢博士說:“我們的生物網(wǎng)絡(luò)分析發(fā)現(xiàn),F(xiàn)OXC1是一系列與癌細(xì)胞轉(zhuǎn)移有關(guān)的基因的主要調(diào)控因子。利用Crispr/Cas9基因編輯技術(shù),我們進(jìn)一步直接展示了超級增強(qiáng)子會驅(qū)使FOXC1的表達(dá)。而更加重要的是,在小鼠的實(shí)驗(yàn)中,我們證實(shí)了FOXC1會促進(jìn)癌細(xì)胞的生長。”
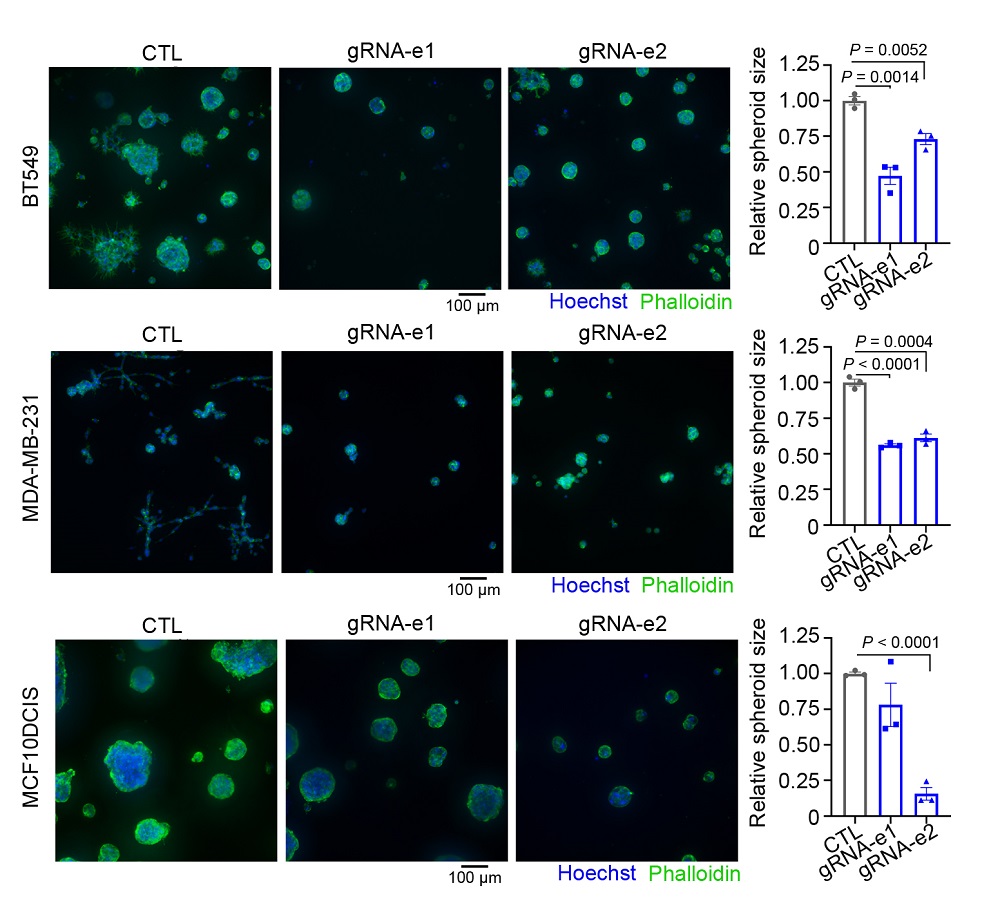
透過對病人臨床樣本進(jìn)行的分析,研究團(tuán)隊(duì)亦發(fā)現(xiàn)了FOXC1的“正調(diào)控”(upregulation)與癌腫瘤的惡化、癌細(xì)胞分裂的速度以及腫瘤浸潤免疫細(xì)胞均有關(guān)連。
與三陰性乳腺癌有關(guān)的另一個(gè)基因
與此同時(shí),研究人員進(jìn)一步利用綜合分析法,發(fā)現(xiàn)了另一個(gè)與三陰性乳腺癌有關(guān)連的基因ANLN。在過往的研究中,ANLN已被證實(shí)與三陰性乳腺癌的復(fù)發(fā)及患者的低生存率有關(guān),而今次研究則發(fā)現(xiàn)若去除ANLN的超級增強(qiáng)子,可以降低蛋白質(zhì)的活躍度,從而減少癌細(xì)胞的生長。錢博士補(bǔ)充:“這些研究成果顯示,表觀遺傳基因圖譜(epigenetic landscape)對于找出影響三陰性乳腺癌的關(guān)鍵因素,具有重大威力,由此可以發(fā)掘出新方法,尋找更多針對這種棘手的乳腺癌的有效治療目標(biāo)。”
乳腺癌是女性最常見的癌癥,根據(jù)全球癌癥數(shù)據(jù)庫Global Cancer Observatory的數(shù)字,2020年乳腺癌占中國婦女所有新發(fā)癌癥的19.9%。而所有乳腺癌個(gè)案中,大約10至15%為三陰性乳腺癌。三陰性乳腺癌與其他乳腺癌最大的分別是這種癌細(xì)胞對雄激素受體(ER)、黃體酮受體(PR)以及一種叫上皮生長素因子(Her2)的蛋白質(zhì),都呈現(xiàn)為陰性,因而被稱為三陰性乳腺癌。故此,三陰性乳腺癌較為“隱形”,而且科學(xué)家至今未能找到有效的“標(biāo)靶”以供藥物去辨別及消滅這種癌細(xì)胞,因此難于治療。
三陰性乳腺癌的患者通常在40至50歲之間發(fā)病,比普通乳腺癌病人的發(fā)病時(shí)間為早。此外,三陰性乳腺癌癌細(xì)胞轉(zhuǎn)移所需的時(shí)間較短,病人通常在接受治療的5年內(nèi)會復(fù)發(fā)。相對于其他種類的乳腺癌,三陰性乳腺癌也較難以預(yù)測治療的結(jié)果。
錢博士寄望這最新的研究能幫助癌癥患者:“我們希望今次的研究成果,能夠?yàn)殚_發(fā)出有效治療三陰性乳腺癌的藥物作出貢獻(xiàn),從而提高病人的生存率。”
香港城大生物醫(yī)學(xué)系的黃昊和胡堅(jiān)楊是論文第一作者,錢博士和王博士則是通訊作者,而同樣來自生物醫(yī)學(xué)系的陳居明博士及張亮博士亦有參與這次研究。今次的研究體現(xiàn)了香港城市大學(xué)與其他醫(yī)學(xué)機(jī)構(gòu)的科研團(tuán)體的跨學(xué)科合作的豐碩成果,來自香港伊利沙伯醫(yī)院以及廣西醫(yī)科大學(xué)附屬腫瘤醫(yī)院的科學(xué)家也曾為研究作出貢獻(xiàn)。

DOI number: 10.1038/s41467-021-22445-0
相關(guān)故事: 更精準(zhǔn)預(yù)測早期結(jié)直腸癌淋巴結(jié)轉(zhuǎn)移風(fēng)險(xiǎn) 香港城大研發(fā)新型腫瘤標(biāo)志物
本文已于 “香港城大研創(chuàng)” 微信公眾號發(fā)布。
Wechat ID: CityU_Research
