精準(zhǔn)基因編輯︰新研發(fā)CRISPR-Cas9蛋白提高基因編輯技術(shù)精準(zhǔn)度
由香港城市大學(xué)(城大)和瑞典卡羅琳醫(yī)學(xué)院合組的一支研究團(tuán)隊(duì),最近成功研發(fā)出一種新的蛋白質(zhì),有助提高基因組編輯過(guò)程中定位的精準(zhǔn)度,相信對(duì)未來(lái)要求高精準(zhǔn)度的人類基因治療可發(fā)揮重要作用。
CRISPR-Cas9(成簇、規(guī)律、間隔、短回文的重複序列及其相關(guān)蛋白9)是一種具有廣泛應(yīng)用前景的基因編輯技術(shù),可用於治療多種遺傳病和開(kāi)發(fā)抗旱農(nóng)作物等,而使用CRISPR-Cas9治療癌癥、血液病和眼疾的臨床試驗(yàn)亦正在進(jìn)行。
原位修復(fù)遺傳缺陷
CRISPR-Cas9使修改或編輯基因變得非常簡(jiǎn)單,因而被公認(rèn)為強(qiáng)大的基因編輯工具。傳統(tǒng)的基因療法是將額外的正常基因引入細(xì)胞,而CRISPR-Cas9的不同之處,在於透過(guò)移除或糾正有問(wèn)題的DNA(脫氧核糖核酸),恢復(fù)正常的基因功能,原位「修復(fù)」遺傳缺陷。

(圖片來(lái)源:美國(guó)國(guó)家衛(wèi)生研究院NIH)
在基因編輯的過(guò)程中,Cas9酶負(fù)責(zé)在進(jìn)行修改之前,要在整個(gè)浩瀚的基因組中搜索並鎖定有問(wèn)題的、或待編輯的目標(biāo)DNA片段(可謂超過(guò)億裡挑一的難度),稱為基因靶向定位。但有時(shí)靶向定位可能不夠精準(zhǔn),或會(huì)在基因組非目標(biāo)的位置修改了DNA,造成脫靶編輯。這種基因組意外改變有機(jī)會(huì)導(dǎo)致嚴(yán)重的後果,如引發(fā)癌癥,就像多年前最初進(jìn)行基因治療試驗(yàn)時(shí)出現(xiàn)的情況。因此,要令CRISPR-Cas9能夠?qū)蚪M進(jìn)行精準(zhǔn)的「分子手術(shù)」,是非常重要的。
現(xiàn)時(shí)CRISPR基因編輯技術(shù)中常用的Cas9酶有兩種版本:SpCas9(來(lái)自化膿性鏈球菌的Cas9核酸酶)和SaCas9(來(lái)自金黃色葡萄球菌的Cas9核酸酶)。在一定程度上,兩者會(huì)出現(xiàn)不精準(zhǔn)或出現(xiàn)脫靶效應(yīng)(即偏離目標(biāo))的情形。先前研究人員已改良了SpCas9,設(shè)計(jì)出SpCas9變體,提高其靶向精準(zhǔn)度。可是,這種SpCas9變體的體積太大,不易被裝入常用於傳遞體內(nèi)基因治療、而容量細(xì)小的腺相關(guān)病毒(adeno-associated virus, AAV)載體中。
相反,SaCas9的體積比SpCas9小得多,很容易被裝入負(fù)載能力有限的AAV載體中,以便在體內(nèi)傳遞基因編輯的「分子手術(shù)刀」。然而,至今仍未有基因組靶向準(zhǔn)確性高的SaCas9。
SaCas9-HF變體大幅提高全基因組靶向精準(zhǔn)度
由香港城大生物醫(yī)學(xué)系兼卡羅琳醫(yī)學(xué)院劉鳴煒復(fù)修醫(yī)學(xué)中心助理教授鄭宗立博士,以及香港城大生物醫(yī)學(xué)系助理教授史家海博士領(lǐng)導(dǎo)的研究團(tuán)隊(duì),針對(duì)普通SaCas9靶向定位不夠精準(zhǔn)的問(wèn)題,最近成功開(kāi)發(fā)出一種CRISPR SaCas9變體,名為SaCas9-HF,能在人類細(xì)胞全基因組內(nèi)精準(zhǔn)靶向定位,而不會(huì)影響在目標(biāo)位置的編輯效率。
研究團(tuán)隊(duì)對(duì)比野生型(即未經(jīng)變異)SaCas9和新型SaCas9-HF的性能,針對(duì)24個(gè)人類基因位置進(jìn)行了嚴(yán)格的測(cè)試。他們發(fā)現(xiàn),對(duì)於在基因組中具有高度相似序列的目標(biāo)基因位置,野生型SaCas9因而容易編輯脫靶,SaCas9-HF則將脫靶效應(yīng)降低約九成;對(duì)於野生型SaCas9較少出現(xiàn)編輯脫靶的目標(biāo)基因位置,SaCas9-HF則幾乎無(wú)法檢測(cè)到脫靶的情況。
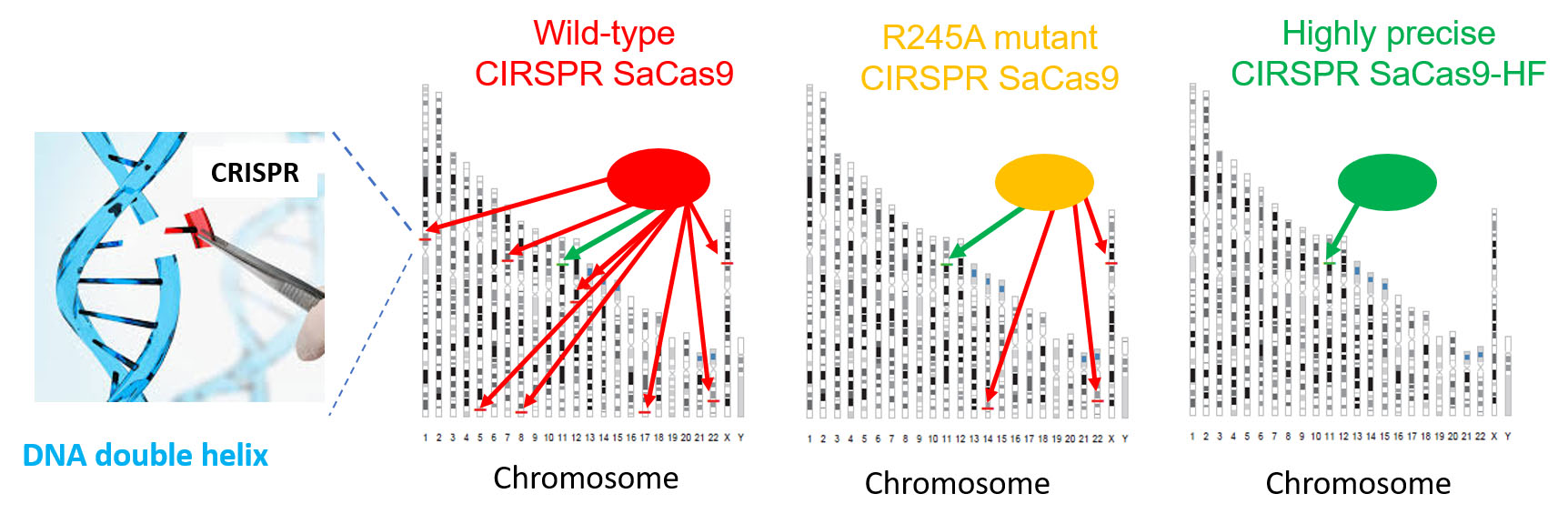
(圖︰鄭宗立博士提供)
SaCas9基因組編輯應(yīng)用的替代方案
「我們研發(fā)出SaCas9-HF,成為野生型SaCas9的替代方案,能在要求高度精準(zhǔn)的基因編輯時(shí)應(yīng)用。這種新型的SaCas9對(duì)於未來(lái)使用AAV載體在體內(nèi)傳送基因組編輯『藥物』或稱為『分子手術(shù)刀』的基因療法特別有用,並將可與最新研發(fā)、能夠『搜索並替換』目標(biāo)基因的CRISPR平臺(tái)『先導(dǎo)編輯』(prime editing)相容。」鄭博士說(shuō)。
此項(xiàng)研究結(jié)果早前在《美國(guó)國(guó)家科學(xué)院院刊》(Proceedings of the National Academy of Sciences,PNAS)上發(fā)表,題為「Rationally engineered Staphylococcus aureus Cas9 nucleases with high genome-wide specificity」。史博士和鄭博士是論文的通訊作者,香港城大生物醫(yī)學(xué)系博士生譚元燕和劉鳴煒復(fù)修醫(yī)學(xué)中心高級(jí)研究助理Athena H. Y. Chu博士是共同第一作者。
其他研究團(tuán)隊(duì)成員包括香港城大生物醫(yī)學(xué)系助理教授熊文君博士、研究助理鮑思羽(現(xiàn)於劉鳴煒復(fù)修醫(yī)學(xué)中心任職)、博士生Hoang Anh Duc和Firaol Tamiru Kebede,以及中山市人民醫(yī)院季明芳教授。
此項(xiàng)研究獲得城大、劉鳴煒復(fù)修醫(yī)學(xué)中心、國(guó)家自然科學(xué)基金委員會(huì)、瑞典研究理事會(huì)、香港政府創(chuàng)新及科技基金、香港醫(yī)療衛(wèi)生研究基金、香港研究資助局、深圳市科技創(chuàng)新委員會(huì)以及深圳市醫(yī)療衛(wèi)生三名工程的支援。
DOI number: 10.1073/pnas.1906843116
